난치성 혈액암인 급성 골수성 백혈병과 만성 골수성 백혈병의 줄기세포 생존 메커니즘이 규명됐다.
한국연구재단은 순천향대 권혁영 교수 연구팀이 종양 줄기세포가 아미노산 결핍 환경에서도 생존할 수 있게 돕는 'DEPTOR' 단백질의 핵심 분자 경로를 규명했다고 3일 밝혔다.

권혁영 교수. 한국연구재단 제공
DEPTOR는 세포 상장과 대사 조절에 중요한 역할을 하는 단백질이다. 연구팀은 이번 연구에서 KIF11 안정화와 대사 적응 조절 기능을 새롭게 규명해 난치성 혈액암 치료의 새로운 전략을 제시했다. KIF11은 세포 분열에 중요한 방추체를 형성하는 단백질로 DEPTOR를 통해 안정화된다.
급성 골수성 백혈병은 조혈 전구세포(특정 세포로 분화되기 이전 단계의 미성숙 세포)의 분화 이상으로 발생, 항암치료나 조혈모세포 이식치료를 하더라도 환자의 5년 생존율이 24%에 그친다.
최근 연구에서 백혈병 세포는 정상 세포와 달리 아미노산 대사에 의존하는 대사적 취약성을 보였고 이 같은 취약성을 표적으로 삼았을 때 암세포 억제가 가능하다는 사실이 밝혀졌다.
하지만 백혈병 줄기세포가 아미노산 결핍 환경에서도 살아남는 적응 메커니즘은 명확하게 규명되지 않아 대사적 취약성을 표적으로 암세포 활성화를 억제할 새로운 치료 전략을 수립하는 데도 한계가 따랐다.
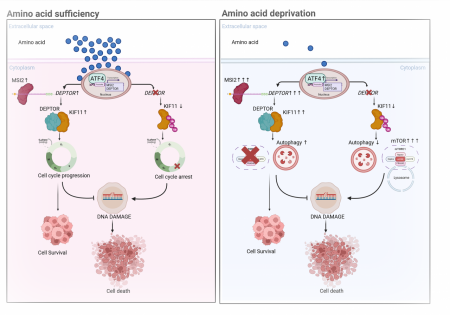
Deptor의 작용 기전. 한국연구재단 제공
이와 관련해 연구팀은 난치성 혈액암에서 아미노산 대사에 관여하는 ▲ATF4(세포 내 스트레스·아미노산 결핍 등에 대한 반응으로 발현이 유도되는 전사인자) ▲MSI2(세포의 증식·분화 및 줄기세포 유지와 관련된 RNA 결합 단백질) ▲DEPTOR ▲KIF11 등 4개 단백질의 상호작용이 백혈병 줄기세포가 대사 스트레스 환경에서도 생존하게 하는 핵심 기전임을 규명했다.
또 이를 억제했을 때 종양 세포를 선택적으로 차단할 수 있다는 사실을 밝혀냈다.
연구팀은 분자 생물학적 기법과 환자 세포, 동물 모델 연구를 통해 아미노산 결핍 환경에서 DEPTOR가 KIF11을 안정화해 mTOR(세포 성장·증식·생존·대사 및 자가 포식 조절을 담당하는 단백질 키나아제 복합체) 조절과 대사 적응을 가능하게 하며 이를 통해 백혈병 세포가 DNA 손상과 세포사멸을 회피한다는 새로운 원리도 제시했다.
실제 실험에서 DEPTOR가 결핍된 조혈모세포에서는 아미노산이 부족할 때 DNA 손상과 세포사멸이 크게 증가했고, 환자 세포와 동물 모델에서도 DEPTOR 억제가 백혈병 진행을 억제하는 것으로 확인했다.
반면 정상 조혈모세포에는 영향이 적어 DEPTOR가 선택적 치료 타깃이라는 것이 입증됐다. 무엇보다 환자 데이터 분석에서 DEPTOR 발현이 높을수록 생존율이 낮아지는 것으로 확인돼 임상적 의의를 뒷받침했다.
권 교수는 "이번 연구는 백혈병은 물론 다른 암종에도 적용 가능해 차세대 항암치료 개발의 토대가 될 것으로 기대된다"고 말했다.
대전=정일웅 기자 jiw3061@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>