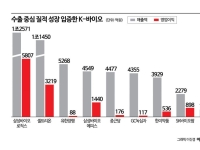
GC셀 "美 아티바, NK세포치료제 임상 3상 진입"
3억달러 대규모 자금 조달
GC셀의 NK세포 제조 기술을 기반으로 설립된 아티바의 NK세포치료제 'AlloNK'(AB-101)가 임상 3상에 진입한다.
GC셀은 미국 관계사 아티바가 개발 중인 AB-101가 임상 3상에 진입하고 3억달러(약 4000억 원)의 자금을 조달했다고 11일 밝혔다.
아티바는 미국 식품의약국(FDA)와 단일 등록용 임상 3상 디자인에 합의했다. 통상적인 두번의 임상 3상 대신 단일 결과만으로 품목허가 신청이 가능한 경로다. 올해 하반기 환자 투여를 시작으로 2028년 하반기 주요 데이터를 도출하고, 2029년 허가 신청을 목표로 한다.
아티바는 기존 치료제(b/tsDMARDs)에 반응하지 않는 난치성 류마티스 관절염 환자를 대상으로 진행 중인 임상 2a상에서 유의미한 데이터를 확보했다. 6개월 이상 추적 관찰이 완료된 환자군 중 71%가 ACR50(증상 50% 개선)에 도달했으며, 고감도 분석 결과 평가 가능한 RA 환자 28명 전원에서 B세포가 완전 고갈되는 결과가 확인됐다고 회사 측은 밝혔다.
아티바는 쇼그렌 증후군과 전신 경화증에서도 초기 데이터가 긍정적으로 나타남에 따라 다른 적응증에 대해서도 안전성 데이터베이스를 구축하는 데 FDA와 합의했다고 밝혔다.
아티바는 보통주와 선납 워런트 발행을 통해 약 3억달러 규모의 자금을 조달했다고 발표했다. 자금 공모에는 헬스케어 전문 투자기관뿐 아니라 원천기술 파트너사인 GC셀과 녹십자홀딩스가 참여했다.
꼭 봐야 할 주요 뉴스
!['숨만 쉬어도 월100' 단칸방서 매일 라면…"결국 도파민에 현실 도피"[위기의 대학생]⑥](https://cwcontent.asiae.co.kr/asiaresize/93/2026051210083259001_1778548113.jpg) '숨만 쉬어도 월100' 단칸방서 매일 라면…"결국 ...
'숨만 쉬어도 월100' 단칸방서 매일 라면…"결국 ...
확보된 자금은 AlloNK 류마티스 관절염 임상 3상 운영과 글로벌 80개 이상 임상 사이트 확장, 2029년 허가 신청까지의 운영 자금으로 투입될 예정이다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>















![[위기의 대학생]④고립 끝에 다가오는 마약 유혹](https://cwcontent.asiae.co.kr/asiaresize/308/2026051207033535043A.jpg)
![[블룸버그 칼럼] '반도체 불장' 뒤 한국 증시의 현실](https://cwcontent.asiae.co.kr/asiaresize/308/2026051214545528801A.jpg)
![[시론]'생산적 부동산'을 위한 조건](https://cwcontent.asiae.co.kr/asiaresize/308/2026051207312297108A.jpg)
![[기자수첩]"빅테크 들러리" 자조하는 카드사, '데이터'로 판 뒤집어라](https://cwcontent.asiae.co.kr/asiaresize/308/2026051210425227045A.jpg)