유럽도 바이오시밀러 임상 간소화…K-바이오시밀러 물들어온다
美·韓 이어 유럽도 임상 간소화 흐
유럽의약품청(EMA)이 바이오시밀러 임상 절차를 간소화하는 권고 보고서를 채택함에 따라 개발 과정이 대폭 단축될 전망이다. 미국과 한국 등 주요 국가 역시 이 같은 규제 완화에 동참하면서 셀트리온·삼성바이오에피스 등 국내 바이오 기업들의 실질적인 수혜가 예상된다.
1일 한국바이오협회 바이오경제연구센터에 따르면 유럽의약품청 산하 약물사용자문위원회(CHMP)는 지난달 27일 바이오시밀러 임상 간소화에 대한 보고서를 채택했다. 유럽 연합 내 특정 바이오시밀러 의약품 개발 및 승인에 요구되는 임상 데이터의 양을 축소하는 것이 이번 보고서의 핵심 목적이다. 통상적으로 의약품의 임상 및 안전성 자료를 심사해 승인 권고를 내리는 CHMP의 결정은 사실상 승인으로 해석되는 경우가 많아 그 영향력이 크다.
지금까지 바이오시밀러 승인을 받기 위해서는 비교성 가능 데이터와 시험관 내 비임상 데이터를 비롯해 약동학, 약력학, 안전성 및 효능 등을 종합적으로 입증하는 비교 임상시험이 요구됐다. 그러나 분석 과학의 발전과 더불어 광범위한 규제 경험이 축적됨에 따라, 비교 임상 효능 및 안전성 데이터의 필요성이 새롭게 재평가되고 있다. 최첨단 분석 방법을 활용하여 물리화학적 및 기능적 특성에서 오리지널 의약품과의 유사성이 철저하게 입증된 바이오시밀러의 경우, 향후 비교효능임상시험(CES)이 승인 과정에서 요구되지 않을 것으로 예상된다.
다만, 비교 임상 약물동태학(PK) 연구는 여전히 바이오시밀러 개발의 필수 요소로 유지돼 안전성과 면역원성 데이터를 제공하는 역할을 수행한다. 특정 조건 하에서는 제한된 임상 데이터 패키지만으로도 분석 수준에서 입증된 유사성을 근거로 의약품 승인을 허용하게 된다. 이는 약물의 본질적인 효능과 안전성을 저해하지 않으면서도 전체 개발 과정을 크게 간소화할 수 있는 장점을 지닌다. EMA는 보고서를 통해 "맞춤형 임상 접근 방식이 대부분의 바이오시밀러 후보 물질 개발에 폭넓게 적용될 수 있을 것"이라고 내다봤다.
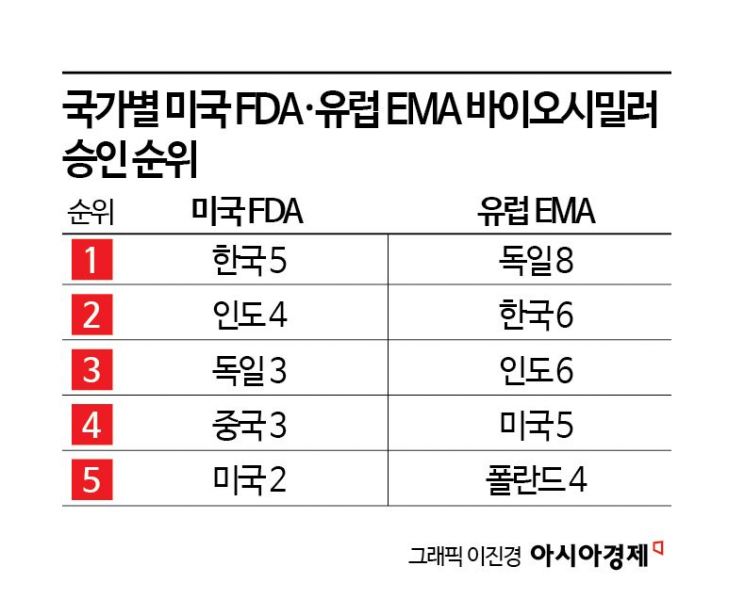
유럽 내 규제 변화는 바이오시밀러를 주력으로 하는 국내 제약 바이오 기업들에게 구체적인 수혜로 이어질 것으로 보인다. 한국바이오협회 바이오경제연구센터가 집계한 자료에 따르면, 올해 3월 말 기준으로 EMA의 허가를 유지하고 있는 바이오시밀러는 총 144개 품목이다. 앞서 허가된 전체 164개 품목 중 효력이 상실되거나 자진 철회된 20개를 제외한 수치다. 이들의 마케팅허가권자(MAH) 현황을 살펴보면, 셀트리온이 13개 품목, 삼성바이오에피스가 11개 품목을 보유하고 있다. 이는 산도즈, 스타다, 바이오시밀러 콜라보레이션 아일랜드 등 다국적 주요 기업들과 함께 상위 5위권에 포진하는 의미 있는 기록이다. 임상 절차가 축소될 경우 연구개발에 소요되는 비용과 시간을 효과적으로 줄일 수 있어, 다수의 파이프라인을 구축한 셀트리온, 삼성바이오에피스 등 국내 기업들의 사업 운영 효율성이 한층 개선될 수 있다.
꼭 봐야 할 주요 뉴스
 72점에서 92점 나오자 난리 났다…문제 찍으면 답 ...
72점에서 92점 나오자 난리 났다…문제 찍으면 답 ...
EMA는 이번 CHMP 권고에 발맞춰 향후 바이오시밀러 평가에 필요한 세부 지침 등을 개정해 간소화 제도를 본격 시행할 예정이다. 바이오경제연구센터는 "미국과 캐나다, 한국 등 다수의 국가들 역시 바이오시밀러 임상 절차 간소화를 적극적으로 추진하고 있어, 올 한 해는 전 세계 바이오시밀러 임상 및 허가 규제 환경에 큰 변화가 도래하는 분기점이 될 전망"이라고 밝혔다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>










![[럭셔리월드]"임신부터 예약 전쟁"…1200만원 돌잔치 '팔선고시'](https://cwcontent.asiae.co.kr/asiaresize/308/2025071508521145584_1752537130.jpg)






![[초동시각]"많이 오지만 적게 쓴다" 한국 관광의 딜레마](https://cwcontent.asiae.co.kr/asiaresize/308/2026040309512226534A.jpg)
![[리셋정치]대구는 전에 없던 선택을 할 것인가](https://cwcontent.asiae.co.kr/asiaresize/308/2026040307450948181A.jpg)



!["수요 폭증하는데 물량이 없어요"…판 커지자 韓부품사들 날개 달았다[칩톡]](https://cwcontent.asiae.co.kr/asiaresize/309/2026040311254913103_1775183149.jpg)
!["인터넷 끊겼어?" 스마트폰, 노트북 다 먹통…순식간에 70년대로 돌아간 모스크바[시사쇼]](https://cwcontent.asiae.co.kr/asiaresize/309/2026040512061714208_1775358377.jpg)


![벚꽃놀이가 아니라 벚꽃전쟁…양복 입고 회사 대신 공원으로 출근한 직장인들[日요일日문화]](https://cwcontent.asiae.co.kr/asiaresize/309/2026040115333599822_1775025215.png)

!["삼성이 먼저 치고 나간다"…독주 균열 조짐에 긴장한 대만 [대만칩통신]](https://cwcontent.asiae.co.kr/asiaresize/309/2026021016165236782_1770707812.jpg)
![고물가에 눌린 서민들 위안…폴란드엔 '우유 식당' 있다 [맛있는 이야기]](https://cwcontent.asiae.co.kr/asiaresize/309/2026040114153699575_1775020536.jpg)
!["임신부터 예약 전쟁"…1200만원 돌잔치 '팔선고시'[럭셔리월드]](https://cwcontent.asiae.co.kr/asiaresize/309/2026040314423013335_1775194949.jpg)








