"美서 1위, 유럽선 6개 통과"… 양대 바이오시밀러 시장 휩쓴 K-바이오
한국 바이오시밀러(바이오의약품 복제약)가 세계 최대 의약품 시장인 미국과 유럽의 규제 장벽을 잇달아 넘어서며 지배력을 강화하고 있다. 지난해 미국 FDA(식품의약국) 허가 실적 1위를 기록한 데 이어, 유럽에서도 셀트리온이 단일 기업 최다 승인 권고를 기록하는 등 글로벌 시장에서의 지위를 갈수록 높이는 모습이다.
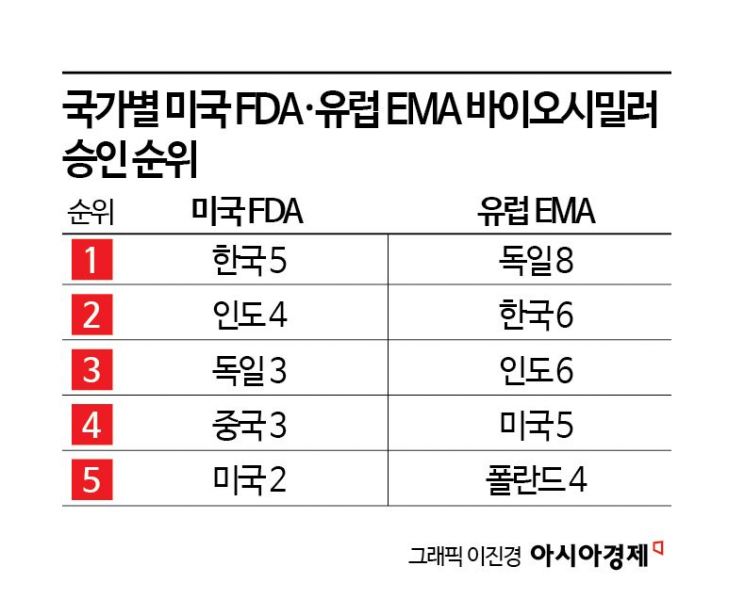
2일 업계에 따르면 지난해 FDA가 승인한 바이오시밀러는 총 18개로, 이 중 셀트리온·삼성바이오에피스 등 한국 기업 제품이 5개(약 28%)를 차지했다. 인도(4개), 독일·중국(각 3개), 미국(2개) 등을 제치고 2년 연속 1위다. 누적 승인 건수에서도 한국은 총 19개를 기록하며, '안방'인 미국 기업(28개)을 턱밑까지 추격했다. 이는 전통의 제약 강국인 스위스·독일 등을 앞서는 수치로, 미국 시장 내에서 K바이오시밀러의 위상이 주류로 자리 잡았음을 시사한다.
셀트리온은 지난해 1월 류머티즘 관절염 치료제 '악템라'의 바이오시밀러인 '앱토즈마'의 승인을 시작으로, 3월에는 골다공증 치료제 프롤리아·엑스지바의 바이오시밀러인 '스토보클로'와 '오센벨트', 그리고 하반기에는 안과 질환 치료제 아일리아의 바이오시밀러 '아이덴젤트'와 천식 치료제 졸레어 바이오시밀러 '옴리클로'까지 잇따라 허가받았다. 특히 '옴리클로'는 FDA로부터 상호 교환 가능한 바이오시밀러로 지정돼 약국에서 의사 처방 없이 오리지널 의약품을 대체할 수 있는 강력한 경쟁력을 확보했다.
삼성바이오에피스 역시 지난해 2월, 골 질환 치료제 프롤리아와 엑스지바의 바이오시밀러인 '오스포미브'와 '엑스브릭'의 FDA 승인을 획득하며 포트폴리오를 강화했다. 삼성바이오에피스는 이번 승인으로 미국 내 승인 제품 수를 10종 이상으로 늘리며 현지 시장 공략의 고삐를 죄고 있다.
유럽 시장에서의 성과도 두드러진다. 유럽의약품청(EMA)과 유럽연합집행위원회(EC)의 문턱을 넘은 국산 바이오시밀러는 지난해 기준 총 6종에 달한다. 독일 8건에 이어 허가 건수 기준으로 유럽 시장에서는 2위다.
셀트리온은 지난해 EMA 산하 약물사용자문위원회(CHMP)로부터 ▲앱토즈마(류머티즘 관절염) ▲아이덴젤트(안과 질환) ▲스토보클로·오센벨트(골 질환) 등 4종에 대해 한꺼번에 '승인 권고'를 획득했다. CHMP의 권고는 사실상 최종 승인을 의미하는 것으로, 단일 기업이 4개 제품에 대해 동시에 허가 권고를 받은 것은 이례적인 기록이다. 삼성바이오에피스도 지난해 '오보덴스'와 '엑스브릭' 2종의 유럽 허가를 따냈다. 이로써 삼성바이오에피스는 유럽 내 승인 제품을 총 11종으로 늘렸으며, 셀트리온 역시 이번 4종의 승인으로 11종의 포트폴리오를 완성하게 됐다. 양사가 유럽 규제당국으로부터 인정받은 제품만 20종이 넘는 셈이다.
업계는 이번 성과가 단순한 허가 건수 증가를 넘어, 올해부터 본격화될 인도 등 신흥국 제약사들의 추격을 따돌릴 결정적 계기가 될 것으로 보고 있다. 셀트리온과 삼성바이오에피스는 다국적 제약사 못지않은 방대한 임상 데이터와 포트폴리오 다양성을 확보했다. 셀트리온은 이번 4종 추가로 자가면역질환을 넘어 안과, 골 질환 등 신규 영역으로 파이프라인을 대폭 확장했으며, 총 135조원 규모의 글로벌 시장을 타깃하게 됐다.
꼭 봐야 할 주요 뉴스
![이란에 '토마호크' 얼마나 퍼부었길래…일본에 '당장 못 준다' 통보한 미국[미국-이란 전쟁]](https://cwcontent.asiae.co.kr/asiaresize/93/2026040316125413514_1775200375.jpg) 이란에 '토마호크' 얼마나 퍼부었길래…일본에 '당...
이란에 '토마호크' 얼마나 퍼부었길래…일본에 '당...
바이오 업계 관계자는 "미국에서는 오리지널 의약품과 교차 처방이 가능한 '상호교환성' 인증을, 유럽에서는 현지 법인을 통한 '직판 체제'를 무기로 수익성을 극대화하고 있다"며 "압도적인 허가 데이터와 시장 선점 효과 덕분에 당분간 K바이오시밀러의 독주 체제는 공고할 것"이라고 전망했다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>



![[인터뷰]정익중 "국내입양과 출산은 다르지 않다"](https://cwcontent.asiae.co.kr/asiaresize/308/2026031121432271388_1773233002.jpg)
![[단독]입양 대기아동 年평균 300명…'해외입양 0명' 해법은](https://cwcontent.asiae.co.kr/asiaresize/308/2026033008152494888_1774826125.jpg)

!["일은 짧고 굵게"…15분 보고제 도입하는 정부[비주얼뉴스]](https://cwcontent.asiae.co.kr/asiaresize/308/2026040315430613475_1775198586.png)




![[기자수첩]정부-소상공인 '빈수레' 간담회, 이럴거면 왜 했나](https://cwcontent.asiae.co.kr/asiaresize/308/2026040309395296812A.jpg)
![[초동시각]"많이 오지만 적게 쓴다" 한국 관광의 딜레마](https://cwcontent.asiae.co.kr/asiaresize/308/2026040309512226534A.jpg)
![[리셋정치]대구는 전에 없던 선택을 할 것인가](https://cwcontent.asiae.co.kr/asiaresize/308/2026040307450948181A.jpg)









!["한달 200만원 들지만 죽는 병은 아니니까"…'우리가 만나 다행'이란 입양가족[잊힌 아이들]⑫](https://cwcontent.asiae.co.kr/asiaresize/309/2026040113464999528_1775018809.jpg)

!["전기요금부터 다 오를 것이다" 트럼프 대국민 연설에 떠는 뉴욕[르포]](https://cwcontent.asiae.co.kr/asiaresize/309/2026040307320212351_1775169122.jpg)




![이란에 '토마호크' 얼마나 퍼부었길래…일본에 '당장 못 준다' 통보한 미국[미국-이란 전쟁]](https://cwcontent.asiae.co.kr/asiaresize/309/2026040316125413514_1775200375.jpg)








