'24년간 상업화 無' 제넥신 "빈혈 신약, 조만간 상용화"
닐 워마 제넥신 대표 인터뷰
GX-E4 1~2년 내·GX-H9 25년 출시 기대
GX-188E, 조건부 승인 신청 신중히 결정할 것
최근 주가 상황은 '저평가'… "기회될 것"
"제넥신의 다양한 파이프라인 중 시장에 출시될 만한 잠재력이 가장 높은 파이프라인 4개를 골랐다. 이 중 첫 상용화가 1~2년 내에 기대되고, 2025년 다음 파이프라인의 출시도 전망하고 있다."
'24년째 상업화된 신약이 없는 회사'. 바이오벤처 제넥신 제넥신 close 증권정보 095700 KOSDAQ 현재가 2,945 전일대비 65 등락률 -2.16% 거래량 75,537 전일가 3,010 2026.06.10 12:53 기준 관련기사 주도주 흔들리자…투심은 ‘교체’와 ‘유지’ 사이 코스피, 외인·기관 순매수 전환에 3200선 회복 '눈앞' 제넥신, EPD바이오 합병해 TPD 기술 강화…최재현·홍성준 각자대표 예고 에 씌워진 오명이다. 이에 아시아경제와 만난 닐 워마 제넥신 대표는 "1~2년 내에 만성신장질환 관련 지속형 빈혈증 치료제 'GX-E4'의 상용화가 기대된다"며 "시급한 대처를 통해 빠르게 제품을 시장에 출시하는 변화를 이끌어내겠다"고 밝혔다.
노바티스, 미국 오펙사, 중국 아이맵 등 다양한 해외 제약·바이오 회사애서의 근무 경험을 가진 워마 대표는 2022년 5월 제넥신에 대표로 합류했다. 워마 대표는 "탄탄한 과학적 기반과 경영진, 많은 후기 파이프라인이 개발돼있다는 점이 매력적으로 느껴졌다"고 합류 계기를 설명했다.
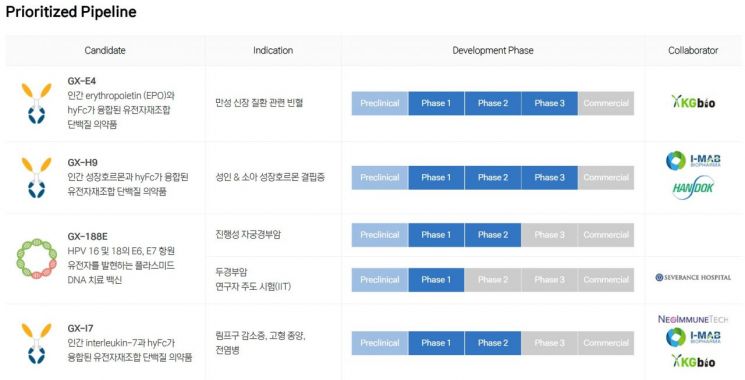
워마 대표는 본인의 취임 후 제넥신에 생긴 가장 큰 변화이자 성과를 '집중'으로 꼽았다. 제넥신의 광범위한 파이프라인 중 당장 집중해야 할 가장 잠재력이 높은 파이프라인 4개를 추렸기 때문이다. 이들이 GX-E4와 암 치료 DNA 백신 'GX-188E', 장기 지속형 성장호르몬 'GX-H9', 림프구 감소증 치료제 'GX-I7'이다. GX-188E 외에는 제넥신의 지속형 단백질 치료제 플랫폼인 하이브리드 Fc(hyFC)가 적용됐다. 워마 대표는 "개발 단계와 시장성을 기준으로 했다"며 "임상 2~3상에 진입해 위험 요인이 상쇄 또는 극복돼있고, 경쟁 제품 대비 차별화가 가능한 파이프라인"이라고 설명했다.
이 중 상용화가 가장 임박한 건 GX-E4다. 적혈구형성인자(EPO)를 hyFc 플랫폼에 접목시켰다. 인도네시아 현지 합작 법인인 KG바이오에 기술을 이전해 2020년부터 한국·인도네시아를 포함한 7개국 다국가 임상 3상이 진행 중이다. 워마 대표는 "인도네시아에는 이미 생물학적 제제 허가 신청(BLA) 절차가 진행 중"이라며 "1~2년 내에 KG바이오를 통한 상용화가 기대된다"고 말했다. 특히 EPO 시장이 꾸준히 커지는 가운데 이 중 지속형 EPO의 비중이 2028년 63%까지 상승할 것으로 전망되는 만큼 아시아·유럽 시장에서 10%의 점유율만 차지한다면 1억3000만달러(약 1694억원) 규모의 매출 목표가 가능하다.
다음 타자로는 장기 지속형 성장호르몬 GX-H9가 나선다. 국내에서는 한독, 중국에서는 워마 대표의 친정인 아이맵과 협력 하에 연구·개발(R&D)이 진행되고 있다. 중국 내 임상 3상 환자 모집을 지난해 마쳤다. 워마 대표는 "오는 6월께 결과를 받을 수 있을 것"이라며 "내년 1분기에 BLA를 제출하고, 2025년 출시를 기대하고 있다"고 말했다. 중국 내 장기 지속형 성장호르몬 시장은 2020년 100만달러에서 2030년 30억달러 규모로 연평균 43%의 성장이 예상되는 만큼 제넥신이 목표로 하는 약 20%의 시장 점유율만 확보하더라도 연간 6억달러의 매출을 확보할 수 있다.
인유두종 바이러스(HPV)가 원인인 자궁경부암·두경부암을 적응증으로 하는 암 치료 백신 GX-188E 역시 자궁경부암은 23%, 두경부암은 10%의 연평균 성장이 예상되는 고성장 시장이다. 자궁경부암 대상 키트루다와의 병용 투여 임상 2상에서 전체생존기간(OS)이 키트루다 단일 요법의 9개월 대비 16.7개월로 2배가량 증가했고, 객관적 반응률(ORR) 35%, 완전 관해 10% 등의 긍정적 결과를 확인했다.
다만 워마 대표는 연내로 기대됐던 국내 조건부 허가 신청에 대해서는 신중한 자세를 취했다. 그는 "국내 조건부 승인도 중요하지만 시장 규모에 대한 고민이 있다"며 "조건부 승인에 매달리기보다는 글로벌 전략의 틀에 조건부 승인을 맞출 필요가 있다"고 말했다. 국내 조건부 승인에 연연할 경우 오히려 글로벌 임상 3상이 늦어지며 해외 진출의 적기를 놓칠 수 있는 만큼 다양한 검토를 하겠다는 복안으로 풀이된다.
![서울 강서구 마곡에 위치한 제넥신의 신사옥 '제넥신 프로젠 바이오 이노베이션 파크'(왼쪽 건물). 오른쪽은 관계사인 한독의 연구소인 '한독 퓨쳐 콤플렉스'다. [사진=이춘희 기자]](https://cphoto.asiae.co.kr/listimglink/1/2023033001393571830_1680107974.jpg)
서울 강서구 마곡에 위치한 제넥신의 신사옥 '제넥신 프로젠 바이오 이노베이션 파크'(왼쪽 건물). 오른쪽은 관계사인 한독의 연구소인 '한독 퓨쳐 콤플렉스'다. [사진=이춘희 기자]
원본보기 아이콘제넥신의 다음 스텝은 글로벌 진출이다. 이에 올해 하반기에 미국 샌디에이고에 현지 사무소를 마련할 예정이다. 앞서 아이맵의 나스닥 상장을 이끌었던 워마 대표의 경험에서 나온 노하우기도 하다. 그는 "미국 진출을 통해 우수한 연구 인력, 거대 투자자본에 대한 접근성이 높아진다"며 "아이맵에서도 샌디에이고 현지 사무소를 통해 회사를 미국에 소개하고, 투자자들의 눈길을 이끌어 상장에 성공했다"고 전했다. 나스닥 이중 상장에 대해서는 "중장기적 목표"라며 "계획을 세워나가는 한편 시장 상황을 지켜보면서 검토하겠다"고 말했다.
재정 면에서는 지난해 말 852억원의 유상증자를 통해 확보한 자금을 연구개발(R&D)에 집중 투자하는 한편 비용 감축을 위해 최대한의 노력을 기울이고 있다고 전했다. 워마 대표는 "지금 시장 상황에서 유상증자를 추진하는 게 민감한 움직임일 수 있어 최대한 미뤄왔지만 R&D 자금이 거의 소진돼 결단을 내렸다"며 "어렵게 조달한만큼 임상과 상용화에 효과적으로 사용하겠다"고 말했다. 이어 "내부 운영 지원 업무를 통합하는 등 업무 효율은 높이고 비용은 줄이는 노력을 기울여왔다"며 "사업 개발(BD)과 파트너십 관리 부분에 대해서도 최대한 엄격한 관리를 시행하려 가다듬고 있다"고도 전했다.
꼭 봐야 할 주요 뉴스
![18년 지났는데 시급 여전히 2만원…"누가 일하겠나" 일감 넘쳐도 사람이 없다[K조선업, 사라진 숙련공]①](https://cwcontent.asiae.co.kr/asiaresize/93/2026060915212793252_1780986087.jpg) 18년 지났는데 시급 여전히 2만원…"누가 일하겠나...
18년 지났는데 시급 여전히 2만원…"누가 일하겠나...
최근의 주가 상황에 대해서는 '저평가'라고 봤다. 제넥신 주가는 전날 종가 기준 1만1790원으로 1년 전과 비교해 64.6%, 연초 대비 17.4% 하락한 상태다. 워마 대표는 "저평가 상황이 다른 관점에서는 기회"라며 "여러 글로벌 상업화 계획을 하나씩 완수해나간다면 분명히 주가에 좋은 기회가 될 것이고, 이런 기회를 주주에게 전달하기 위해 최선의 노력을 다하겠다"고 말했다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>
![닐 워마 제넥신 대표가 아시아경제와 인터뷰하고 있다. [사진제공=제넥신]](https://cphoto.asiae.co.kr/listimglink/1/2023033001224171828_1680106962.jpg)
![곪고 곪아 결국 터졌다… '선거의 심판' 그 민낯 [Data Pick]](https://cwcontent.asiae.co.kr/asiaresize/308/2026061008333116549A.jpg)













![손흥민 몸 푸는데…"군대도 안 갔다 온 것들" 막말 논란 어쩌나[2026월드컵]](https://cwcontent.asiae.co.kr/asiaresize/308/2026060918230693501_1780996986.jpg)


![[아경의 창]스코세이지 감독과 AI의 만남](https://cwcontent.asiae.co.kr/asiaresize/308/2026061010353750306A.jpg)
![[초동시각]30개월 빈자리…강원랜드에 필요한 '진짜 전문가'](https://cwcontent.asiae.co.kr/asiaresize/308/2026061010250024551A.jpg)
![[기자수첩]오너의 복귀보다 중요한 것](https://cwcontent.asiae.co.kr/asiaresize/308/2026061009263157211A.jpg)





![손흥민 몸 푸는데…"군대도 안 갔다 온 것들" 막말 논란 어쩌나[2026월드컵]](https://cwcontent.asiae.co.kr/asiaresize/309/2026060918230693501_1780996986.jpg)


![[단독]중국이 장악한 시장에 3000억 베팅하는 정부…국민성장펀드 활용한다](https://cwcontent.asiae.co.kr/asiaresize/309/2026050113551348205_1777611313.jpg)


!['월 13만원' 퇴근 후 용돈벌이로 '우르르' 뛰어들더니…부작용 커졌다[금융현미경]](https://cwcontent.asiae.co.kr/asiaresize/309/2026061012391894490_1781062757.png)
![[속보]이란 매체 "美 이란 공격 진정…상황 평온"](https://cwcontent.asiae.co.kr/asiaresize/309/2026060913442293034_1780980262.png)



![곪고 곪아 결국 터졌다… '선거의 심판' 그 민낯 [Data Pick]](https://cwcontent.asiae.co.kr/asiaresize/307/2026061009353894036_1781051738.png)



