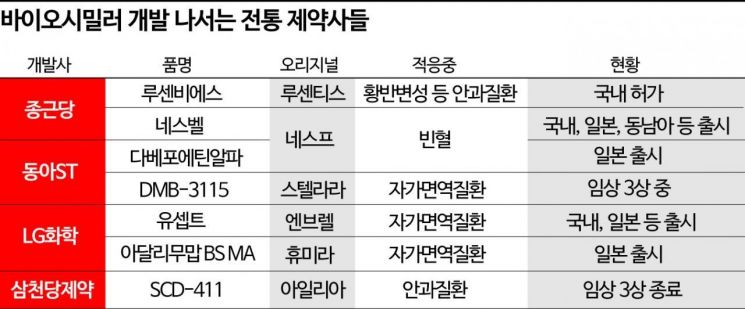
종근당 '루센비에스' 국내 허가
'네스벨'에 이어 두번째 자체 시밀러
전통 제약사들도 연이어 개발·출시
동아ST '다베포에틴알파' 'DMB-3115'
LG화학 '유셉트' '아달리무맙 BS MA'
대부분 일본 등 아시아 국한은 아쉬움
동아ST·삼천당, FDA 승인 임상 중
[아시아경제 이춘희 기자] 셀트리온 , 삼성바이오에피스 등 바이오기업으로 대표돼 온 한국 바이오시밀러(바이오의약품 복제약) 업계에 전통 제약사들이 잇따라 도전장을 던지고 있다. 핵심 바이오의약품들에 대한 바이오시밀러 출시에 연이어 성공하는 가운데 미국 식품의약국(FDA) 허가를 직접 겨냥하는 바이오시밀러도 개발되고 있다.
종근당 은 최근 습성 황반변성 등 안과 질환 치료제인 '루센티스'의 바이오시밀러 '루센비에스'의 국내 허가를 받았다. 특히 습성 황반변성뿐만 아니라 당뇨병성 황반부종, 당뇨성 망막병증 등 루센티스가 국내에서 승인받은 모든 적응증(full-label)에 대한 승인을 받는 데 성공했다. 종근당은 국민건강보험 등재 절차를 거쳐 조만간 제품 출시에 나설 예정이다. 이로써 루센비에스는 2019년 출시된 '네스벨'에 이어 종근당이 자체 개발한 두 번째 바이오시밀러가 됐다. 빈혈 치료제 '네스프'의 바이오시밀러인 네스벨은 현재 국내 외에도 일본, 동남아시아, 중동 등에 진출한 상태다.
커지는 바이오시밀러 시장 잡아라… 아시아 시장 중심 공략
종근당 외에도 동아에스티 , LG화학 , 삼천당제약 등 전통 제약사들도 최근 바이오시밀러 시장 개척에 활발히 나서고 있는 모습이다. 동아에스티 역시 네스프 바이오시밀러 '다베포에틴알파'를 개발해 일본에서 판매하고 있다. 임상 1상을 마친 후 일본 삼화화학연구소(SKK)에 일본 내 개발 및 판매 권한을 이전했다. 지난해에는 연 매출 100억원을 넘어서기도 했다.
LG화학은 자가면역질환 치료제인 '엔브렐'과 '휴미라'의 바이오시밀러인 '유셉트'와 '아달리무맙 BS MA'를 개발해 판매하고 있다. 바이오시밀러 시장이 형성되기도 전인 2010년부터 유셉트의 개발에 착수해 2018년 일본과 한국에 출시했다. 특히 일본에서는 엔브렐 바이오시밀러 중 최초로 시장에 출시에 성공하며 지난 1분기 기준 '에타너셉트' 성분 시장 점유율 40%를 달성한 상태다. 아달리무맙 BS MA 역시 지난해 일본에 출시해 시장 확대를 노리고 있다.
다만 아직 전통 제약사들의 바이오시밀러 시장 진출이 활발하다고 보기는 어렵다. 대부분 제품의 출시가 아직은 국내와 일본, 동남아, 중동 등 아시아 지역에만 집중돼 이뤄지고 있기 때문이다. 의약품 세계 최대 시장인 미국에서 허가된 국산 바이오시밀러는 여전히 셀트리온('램시마', '트룩시마', '허쥬마', '베그젤마')과 삼성바이오에피스('에티코보', '렌플렉시스', '하드리마', '온투르잔트', '바이우비즈')가 만든 바이오시밀러뿐이다. 이에 임상 단계로부터 미국 시장을 겨냥하고 있는지를 눈여겨봐야 한다는 지적도 나온다.
삼천당제약은 안과 질환 치료제인 '아일리아'의 바이오시밀러로 개발 중인 'SCD-411'의 임상 3상을 최근 종료했다. FDA로부터 임상시험계획(IND)을 승인받아 미국, 일본 등 15개국에서 황반변성 환자 576명을 대상으로 임상을 진행했다. 삼천당제약은 내년 1월께 임상 3상 최종 보고서를 받은 후 일본, 미국, 한국, 유럽 등에 허가 신청을 진행할 계획이다.
동아에스티 역시 내년부터 특허가 만료되는 자가면역질환 치료제 '스텔라라'의 바이오시밀러 'DMB-3115'의 임상 3상을 미국을 포함해 진행 중이다. 미국 외 폴란드, 에스토니아 등 유럽 지역에서 판상 건선 환자 605명의 모집을 지난해 말 완료하고 올해 안으로 임상을 마칠 예정이다.
이춘희 기자 spring@asiae.co.kr
꼭 봐야할 주요뉴스
!["유산? 내가 다 쓰고 간다"…"실버타운? 내 돈 쥐고 '보증금 0원' 호텔 살란다"[부동산AtoZ]](https://cwcontent.asiae.co.kr/asiaresize/93/2026021913144345005_1771474484.jpg) "유산? 내가 다 쓰고 간다"…"실버타운? 내 돈 쥐...
마스크영역
"유산? 내가 다 쓰고 간다"…"실버타운? 내 돈 쥐...
마스크영역
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>









!["남들 10% 벌 때 난 20% 번다" 수익률 톱10 '싹쓸이'한 레버리지 ETF[재테크 풍향계]](https://cwcontent.asiae.co.kr/asiaresize/269/2026021309362441835_1770942984.jpg)








![[리셋정치]무기징역 선고는 상식적인 판결](https://cwcontent.asiae.co.kr/asiaresize/269/2026022007425526843A.jpg)
![[시시비비] 중복상장, 어설픈 관치(官治)의 그림자](https://cwcontent.asiae.co.kr/asiaresize/269/2026022011022027364A.jpg)
![[논단]수평선을 걷는 인간, 수직 상승하는 AI](https://cwcontent.asiae.co.kr/asiaresize/269/2026022011062749889A.jpg)


 가장 많이 읽힌 뉴스를 제공합니다. 집계 기준에 따라 최대 3일 전 기사까지 제공될 수 있습니다.
가장 많이 읽힌 뉴스를 제공합니다. 집계 기준에 따라 최대 3일 전 기사까지 제공될 수 있습니다.

![[단독]靑 업무량 역대 최고 수준…1인당 초과근무 月62시간](https://cwcontent.asiae.co.kr/asiaresize/269/2026022007361945741_1771540579.jpg)






