자폐·발달장애 치료약 개발 실마리 찾았다
기초과학연구원 김은준 연구팀, TANC2 단백질 결손 매커니즘 규명
[아시아경제 김봉수 기자] 국내 연구진이 특정 단백질의 결손이 자폐나 뇌 발달장애를 유발한다는 사실을 밝혀냈다. 치료제 개발에 실마리가 될 전망이다.
기초과학연구원(IBS)은 시냅스 뇌질환 연구단 김은준 단장 연구팀이 TANC2 단백질 결손이 자폐 및 뇌 발달장애를 유발하는 매커니즘을 규명했다고 11일 밝혔다.
자폐증(Autism spectrum disorders)은 뇌 발달장애의 한 종류로서, 세계 인구의 약 2%가 앓고 있다. 뇌의 발달은 세포 내 다양한 신호전달(signaling) 체계에 의해 조절된다. 그중 ‘mTOR 신호전달’은 신경세포를 포함한 대부분 세포의 발달과 기능을 제어한다. 여기에는 대사 장애, 뇌 발달장애 등 다양한 질환이 관련되어 있다고 알려져 있다. 그러나 신경계에서의 mTOR 조절 기전은 이제까지 알려진 바가 거의 없었다.
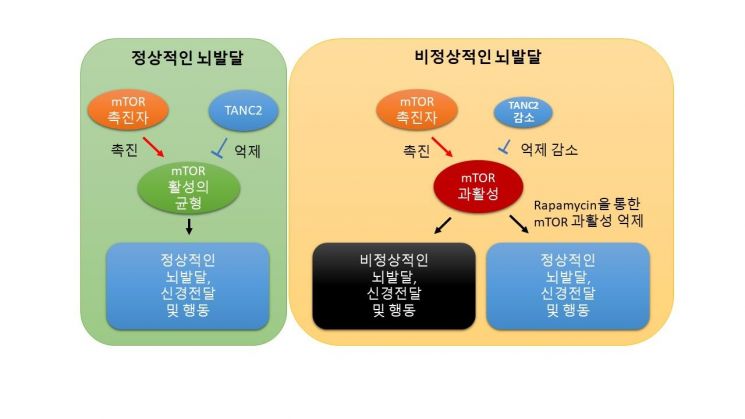
시냅스 뇌질환 연구단은 이전 연구에서 ‘TANC2 단백질’이 정상적인 뇌 발달에 필수적임을 규명했다. 이후 다양한 임상연구를 통해 TANC2와 자폐 및 뇌 발달장애의 연관 가능성이 제기되었다. 다만 정확한 발병기전을 밝히지는 못했었는데, 연구팀은 이번 연구에서 TANC2 단백질이 mTOR 단백질의 직접 억제자(negative regulator)로서 뇌 발달 및 기능을 조절함을 규명했다.
연구진은 TANC2 단백질과 mTOR 신호전달의 관계를 파악하고자 TANC2 발현이 절반으로 줄어든 자폐증 생쥐 모델을 제작했다. 실험 결과 TANC2 단백질 결손이 mTOR 신호전달 단백질의 비정상적 과활성화로 이어져 시냅스 및 기억·학습 등의 뇌 기능이 저하됐다. 이때 mTOR 저해 약물인 라파마이신(Rapamycin)을 투여하면 시냅스 및 뇌 인지 기능이 정상으로 회복됐다. TANC2 단백질이 mTOR 신호전달 단백질을 저해하여 뇌 기능을 조절한다는 의미다.
인체의 신경세포에서 TANC2가 줄어들면 mTOR 신호전달체계가 비정상적으로 활성화됨도 발견했다. 인간의 신경계에서도 TANC2가 mTOR 저해인자로서 뇌 발달 및 뇌 기능을 조절하는 것이다.
김은준 단장은 “이번 연구로 최근 자폐 및 뇌 발달장애의 원인으로 부상한 TANC2 유전자 변이의 발병 메커니즘을 밝혔다”며,“후속 연구를 통해 mTOR 신호전달 억제제를 TANC2 유전자 돌연변이에서 기인한 자폐 및 뇌 발달장애의 치료에 활용할 수 있을 것”이라고 전했다.
꼭 봐야 할 주요 뉴스
 지금 주문하면 4~5년 뒤에나 받는다…"그 공장 첫 ...
지금 주문하면 4~5년 뒤에나 받는다…"그 공장 첫 ...
이번 연구 결과는 국제 학술지 네이처 커뮤니케이션즈(Nature Communications, IF 12.121) 온라인판에 이날 게재됐다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>

![[금융현미경]두 달째 결론 못 내는 '홍콩 ELS' 과징금…딜레마 빠진 금융당국](https://cwcontent.asiae.co.kr/asiaresize/308/2026041414402525462_1776145225.png)

![[기자수첩]공감 없이 ‘에너지 태산’은 없다](https://cwcontent.asiae.co.kr/asiaresize/308/2026041513531538594A.jpg)
![[초동시각]나프타와 석화산업 존재의 의미](https://cwcontent.asiae.co.kr/asiaresize/308/2026041511153582869A.jpg)
![[산업의 맥]위험의 시대, 약가인하와 중동 리스크](https://cwcontent.asiae.co.kr/asiaresize/308/2026041511142177941A.jpg)





















![[실전재테크]GTX-C 호재에 창동·인덕원 꿈틀…주춤하는 양주·의정부](https://cwcontent.asiae.co.kr/asiaresize/309/2026041415373825642_1776148659.jpg)













